31.03.23
Surveillance de l’hygiène : l’embarras du choix
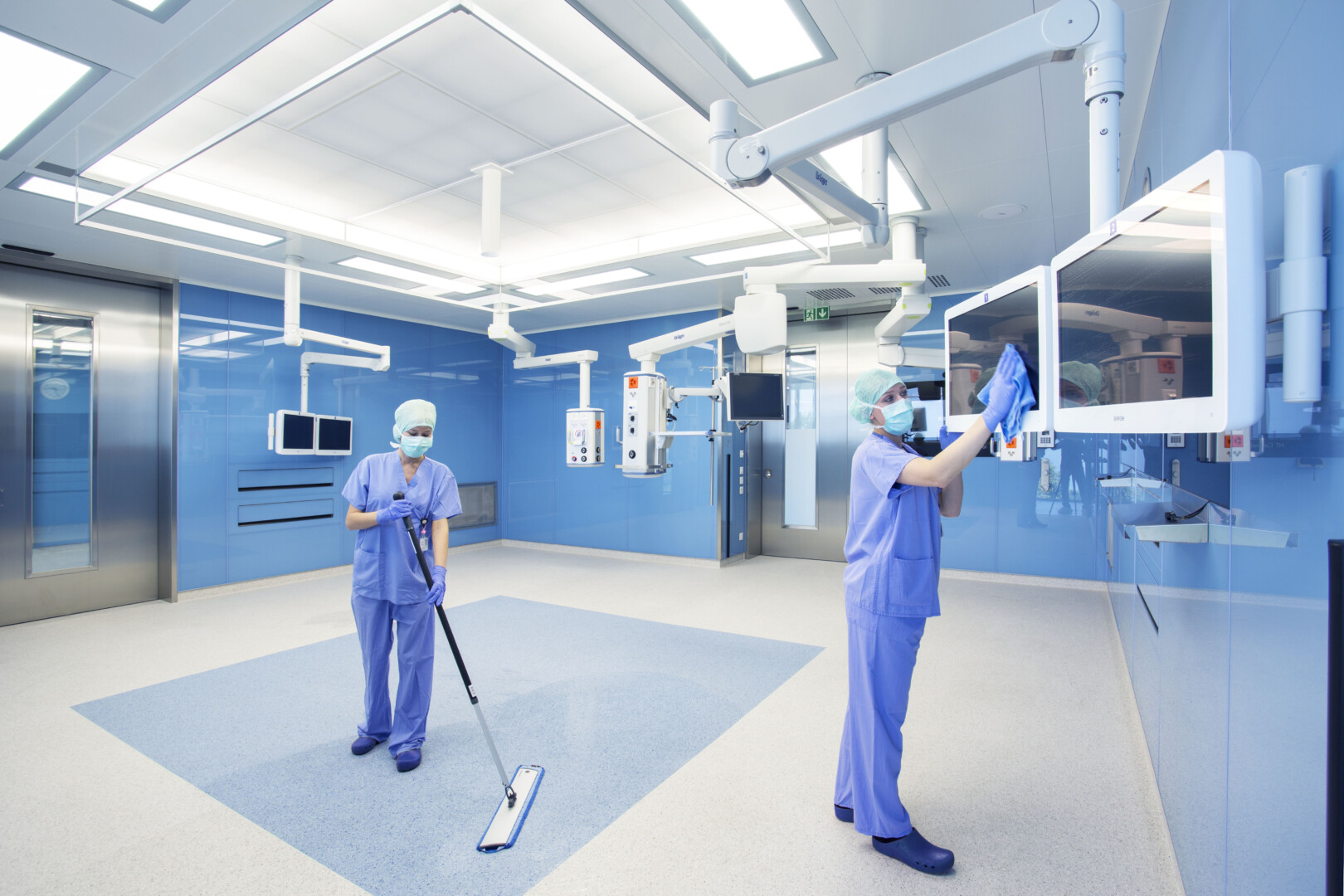
Le monitoring de l'hygiène, ou contrôle de l'hygiène en français, est considéré de manière simplifiée comme la surveillance générale des mesures visant à préserver la santé. Il est utilisé dans les industries pharmaceutiques, biotechnologiques, cosmétiques et alimentaires, ainsi que dans les hôpitaux, les pharmacies, les cuisines collectives et d'autres domaines exigeants en matière d'hygiène pour surveiller l'hygiène des collaborateurs, des produits et des processus.
Résumé
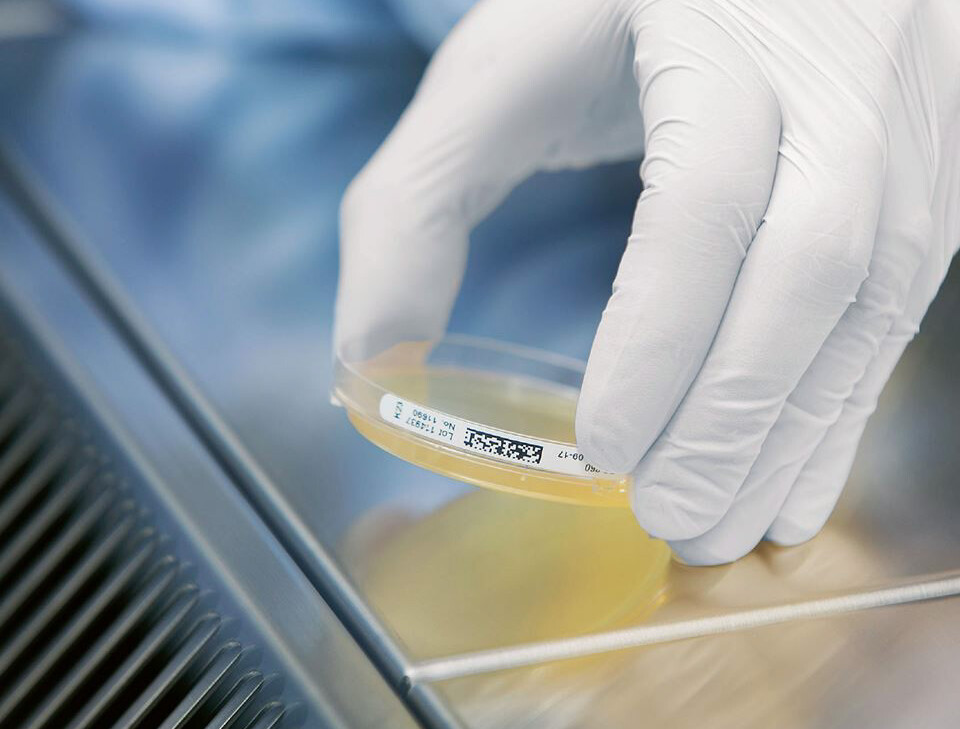
Le monitoring de l’hygiène, ou contrôle de l’hygiène en français, est considéré de manière simplifiée comme la surveillance générale des mesures visant à préserver la santé. Il s’agit en particulier de la surveillance de diverses contaminations microbiologiques qui peuvent entraîner des maladies infectieuses directes et indirectes, des maladies chroniques de différents types, des réactions allergiques et des épidémies.
Les contrôles d’hygiène microbiologiques de diverses salles blanches, comme par exemple dans la production pharmaceutique, les salles d’opération et les chambres de quarantaine, la production alimentaire, les espaces publics et d’autres domaines sensibles sur le plan de l’hygiène, servent à prouver par un monitoring régulier la qualité de la propre gestion de l’hygiène avec des données concrètes et à la corriger si nécessaire.
En fin de compte, le contrôle de l’hygiène confirme l’assurance qualité des produits et des services de toutes sortes, ainsi que les efforts visant à assurer la sécurité des collaborateurs, des patients, des visiteurs et des consommateurs, sans oublier l’environnement proche et l’environnement général.
Surveillance de l’hygiène
Sur la base de la norme européenne EN 17141, « Salles blanches et environnements maîtrisés associés – Contrôle de la biocontamination », – anciennement EN ISO 14698-1:2003 et EN ISO 14698-2:2003 -, un mélange de plaques de sédimentation, de prélèvements par écouvillons/spatules, de mesures actives des germes dans l’air et d’analyses de surface par plaques d’écouvillonnage est utilisé pour la surveillance microbiologique de l’hygiène des sites de production dans les zones réglementées.
Les réglementations exigent la réalisation régulière de monitorings à une fréquence suffisamment élevée pour pouvoir détecter à temps les écarts qui se produisent et pour pouvoir garantir une signification statistique de la collecte des données. La fréquence du monitoring dépend de facteurs tels que la classe BPF de la salle blanche, l’évaluation des risques du processus de production, la conception de la salle blanche, les interactions avec les personnes dans l’environnement direct et les données historiques existantes, qui doivent être évaluées par des experts techniques formés.
Chaque exploitant de salle blanche a la responsabilité de définir sa fréquence de surveillance, de la justifier et de l’adapter régulièrement. Le monitoring de l’hygiène est utilisé dans les industries pharmaceutiques, biotechnologiques, cosmétiques et alimentaires, ainsi que dans les hôpitaux, les pharmacies, les cuisines industrielles et d’autres domaines exigeants en matière d’hygiène pour surveiller l’hygiène des collaborateurs, des produits et des processus.
La méthode de mesure appropriée : l’embarras du choix
Il existe différentes méthodes de mesure pour obtenir les données nécessaires. Selon le type de germes ou de particules infectieuses à mesurer, le volume de prélèvement, la fréquence, la période d’observation ainsi que la méthode appropriée doivent être choisis et réalisés par des spécialistes, et leurs données doivent être soigneusement évaluées et communiquées. Outre les méthodes de mesure microbiologiques classiques basées sur la culture ou les méthodes de détection directes et indirectes de paramètres d’hygiène directs et indirects, il existe également des méthodes microbiologiques rapides et des méthodes de détection microbiologiques alternatives en temps réel.
Dans un laboratoire spécialisé ou « sur place » chez le client
Outre les laboratoires hautement spécialisés dans l’analyse microbiologique d’échantillons ou de paramètres et l’évaluation très spécifique des échantillons prélevés lors des contrôles, d’autres technologies sont disponibles avec des méthodes d’analyse microbiologique « sur place » ou « on-site » pour une correction nettement plus rapide et ciblée des mesures d’hygiène existantes.
Alors que les laboratoires centraux hautement spécialisés peuvent fournir de très bons résultats qualitatifs et quantitatifs avec une grande précision, une limite de détection basse et une excellente spécificité jusqu’au niveau de l’ADN/du génome et de la séquence protéique, les méthodes plus simples de mesures sur site sont généralement moins précises et moins spécifiques. En revanche, les résultats sont disponibles beaucoup plus rapidement et des mesures correctives peuvent être prises beaucoup plus rapidement. Ceci est décisif dans tous les domaines où il n’est pas possible d’attendre plusieurs heures ou plusieurs jours pour obtenir un résultat.
Une combinaison et une expertise d’évaluations spécifiques en laboratoire et de méthodes de mesure sur site plus rapides – souvent moins précises – garantissent une qualité élevée de l’ensemble de la chaîne de prestations – de la collecte et de l’évaluation efficaces, rapides et correctes des données, d’une analyse spécialisée des échantillons, en passant par des conclusions professionnelles, jusqu’à la proposition des mesures de contrôle de l’hygiène à prendre.
En général, le contrôle microbiologique propose un système auto-optimisant sur une base continue, qui identifie, exécute, contrôle ou surveille et adapte. Il s’agit d’un processus cyclique classique d’amélioration continue, dans lequel les principes : Planifier – Exécuter – Contrôler – Agir (PDCA, i.e. Plan, Do, Check and Act).
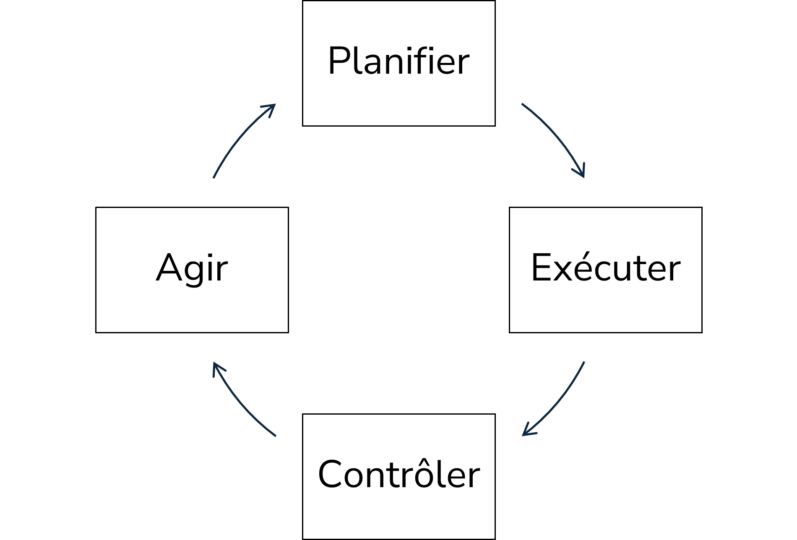
Lors de la création et de la planification d’une solution d’hygiène appropriée d’un système de contrôle microbiologique d’entreprise, une bioanalyse adaptée est la pierre angulaire. Il s’agit d’identifier toutes les sources et voies potentielles de contamination microbiologique, de planifier et de tester les solutions appropriées sur place ou en laboratoire. Pendant la mise en œuvre et l’utilisation, ainsi que pendant les autres phases de l’amélioration continue, les méthodes de mesure rapides sur site peuvent aider à surveiller et à vérifier le concept de mesures choisi, à le maintenir ou à le corriger et donc à l’améliorer.
En résumé, l’avantage ou le bénéfice d’un contrôle adapté de la biocontamination consiste en une combinaison de différents facteurs :
- Choix des analyses appropriées sur place et/ou des confirmations centralisées en laboratoire grâce à des méthodes de mesure microbiologiques adaptées et optimisées ; ceci en tant que combinaison de « rapidité sur place » et de « précision et spécificité » en laboratoire.
- Analyse des données et évaluation des risques ainsi qu’élaboration d’un plan de surveillance spécifique et optimisé pour le système.
- Recommandation compétente en cas d’écarts et prise des mesures correctives appropriées.
- Mais ce qui est décisif, ce sont surtout des temps de réaction courts pour effectuer les analyses nécessaires ainsi que les travaux de correction, de décontamination et d’hygiène avant que des dommages importants ne soient causés aux personnes, aux produits ou à l’environnement.
Mise en œuvre spécifique dans les différentes industries et le secteur de la santé
Il existe un grand nombre de guides différents, notamment pour les secteurs pharmaceutique, biopharmaceutique, des dispositifs médicaux et d’autres secteurs des sciences de la vie, ainsi que pour le secteur de la santé et les hôpitaux et les applications connexes. Tous ces domaines et secteurs ont en commun de posséder et/ou d’utiliser des zones contrôlées et hautement pertinentes en termes de propreté ou d’hygiène.
Dans l’industrie de production pharmaceutique et biopharmaceutique réglementée, il existe déjà de nombreuses normes et directives réglementaires à appliquer. Il s’agit notamment de l’annexe 1 du guide des BPF de l’UE sur la fabrication de médicaments stériles et du guide de la FDA sur la fabrication aseptique. Les réglementations pharmaceutiques européennes et américaines contiennent également quelques instructions sur certains sujets connexes. De nombreux autres documents et articles techniques sont disponibles auprès des associations industrielles, notamment la Parenteral Drugs Association (PDA), l’International Society of Pharmaceutical Engineering (ISPE) et la Pharmaceutical Healthcare Sciences Society (PHSS).
Dans le secteur des soins de santé et des hôpitaux, des directives européennes, y compris des directives sur les tissus et le sang, sont disponibles pour les zones spécialisées et les zones similaires dont la propreté est contrôlée. Des normes et directives nationales sont disponibles pour les salles d’opération spécialisées, les unités d’isolement et les unités pour patients immunodéprimés dans le cadre du contrôle des infections. En outre, les zones aseptiques pour le mélange des médicaments dans les pharmacies hospitalières, les pharmacies radiopharmaceutiques et les laboratoires spécialisés tels que les laboratoires de cellules souches utilisent généralement des documents d’orientation issus de l’industrie des sciences de la vie.
Alors que des règlements et des normes sont disponibles pour la gestion des risques des dispositifs médicaux, comme la norme EN ISO 14971, il existe généralement moins d’instructions pour le contrôle microbiologique d’autres zones contrôlées pour la propreté générale.
Bien qu’il existe des règlements et des normes dans le secteur alimentaire et les secteurs connexes des biens de consommation, par exemple pour les aliments, les boissons et les cosmétiques, il n’existe pas suffisamment de guides pour le contrôle microbiologique dans les zones dont la propreté est contrôlée.
Littérature
- DIN EN 17141:2020: Reinräume und zugehörige Reinraumbereiche – Biokontaminationskontrolle
- DIN EN ISO 14698-1:2003: Reinräume und zugehörige Reinraumbereiche – Biokontaminationskontrolle – Teil 1: Allgemeine Grundlagen
- DIN EN ISO 14698-2:2003: Reinräume und zugehörige Reinraumbereiche – Biokontaminationskontrolle – Teil 2: Auswertung und Interpretation von Biokontaminationsdaten
- EN ISO 14644-1:2015: Reinräume und zugehörige Reinraumbereiche – Teil 1: Klassifizierung der Luftreinheit anhand der Partikelkonzentration
- EN ISO 14644-2:2015: Reinräume und zugehörige Reinraumbereiche – Teil 2: Überwachung zum Nachweis der Reinraumleistung bezüglich Luftreinheit anhand der Partikelkonzentration
- EN ISO 14644-3:2005: Reinräume und zugehörige Reinraumbereiche – Teil 3: Prüfverfahren
- EN ISO 14644-4:2001: Reinräume und zugehörige Reinraumbereiche – Teil 4: Planung, Ausführung und Erst-Inbetriebnahme
- EN ISO 14644-5:2004: Reinräume und zugehörige Reinraumbereiche – Teil 5: Betrieb
- EN ISO 14644-7:2004: Reinräume und zugehörige Reinraumbereiche – Teil 7: SD-Module (Reinlufthauben, Handschuhboxen, Isolatoren und Minienvironments)
- Enzler h-tec Einstleistungen – Angewandte Hygienetechnologien
- ISO 14971, Medical devices – Application of risk management to medical devices
- Point H.A.C.C. (HACCP) system and guidelines for its application. 1995 Codex Alimentarius Commission. Alinorm 97/13. Annex to Appendix II. Joint FAO/WHO Food Standards Programme. Food and Agricultural Organization of the United Nations, Rom, 1995.
- European Commission EudraLex „The Rules Governing Medicinal Products in the European Union“, Volume 4.
- EU Guidelines for Good Manufacturing Practice, Medicinal Products for Human and Veterinary Use, Annex 1 – Manufacture of Sterile Medicinal Products, 25. Nov. 2008
- FDA Guidance for Industry – Sterile Drug Products Produced by Aseptic Processing – Current Good Manufacturing Practice. September 2004.
- IS0 18593:2018: Mikrobiologie der Lebensmittelkette – Horizontales Verfahren für Probenahmetechniken von Oberflächen